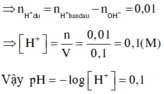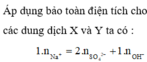Dung dịch X chứa 0,07 mol \(Na^+\),x mol \(SO^{2-}_4\), 0,1 mol \(OH^-\). Dung dịch Y chứ y mol \(^{H^+}\), z mol \(Ba^{2+}\), 0,02 mol \(NO^{^-_3}\).Trộn X với Y,sau khi phản ứng thu được 500ml dd có pH=2 và thu được m gam kết tủa.Tính m

Những câu hỏi liên quan
Dung dịch X chứa 0,07mol Na+, x mol SO42- , 0,01 mol OH-. Dung dịch Y chứa y mol H+, z mol Ba2+, 0,02 mol NO3-. Trộn X với Y, sau khi phản ứng xong được 500ml dung dịch có pH 2 và thu được m gam kết tủa. Tính m A. 0,5825g B. 3,495g C. 0,345g D. 6,99g
Đọc tiếp
Dung dịch X chứa 0,07mol Na+, x mol SO42- , 0,01 mol OH-. Dung dịch Y chứa y mol H+, z mol Ba2+, 0,02 mol NO3-. Trộn X với Y, sau khi phản ứng xong được 500ml dung dịch có pH = 2 và thu được m gam kết tủa. Tính m
A. 0,5825g
B. 3,495g
C. 0,345g
D. 6,99g
A
Dung dịch X. Số mol (SO4)2- = 0,03 mol.
Từ pH = 2 ta tính được số mol H+ = 5. 10-3 mol.
Vậy số mol H+ trong dung dịch Y là : 0,01 + 5. 10-3 = 0,015 mol
Số mol của Ba2+ = 2,5.10-3 mol.
Ba2+ + SO42- ® BaSO4
Vậy khối lượng kết tủa: m = 2,5.10-3.233 = 0,5825 gam.
Đúng 0
Bình luận (0)
Dung dịch X có chứa 0,07 mol ^{Na^+} ; 0,02 mol SO^{2-}_4 và x mol OH^-. Dung dịch Y có chứa ClO^-_4,NO^-_3 và y mol H^+ ; tổng số mol ion trong Y là 0,04. Trộn X và Y được 100ml dd Z. Dung dịch Z có pH ( bỏ qua sự điện li của H_2O ) là ?
Đọc tiếp
Dung dịch X có chứa 0,07 mol \(^{Na^+}\) ; 0,02 mol \(SO^{2-}_4\) và x mol \(OH^-\). Dung dịch Y có chứa \(ClO^-_4\),\(NO^-_3\) và y mol \(H^+\) ; tổng số mol ion trong Y là 0,04. Trộn X và Y được 100ml dd Z. Dung dịch Z có pH ( bỏ qua sự điện li của \(H_2O\) ) là ?
Dung dịch X có chứa 0,07 mol Na+; 0,02 mol và x mol OH-. Dung dịch Y có chứa ; và y mol H+. Tổng số mol và là 0,04 mol. Trộn X với Y thu được 100ml dung dịch Z. Bỏ qua sự điện li của nước, pH của dung dịch thu được là: A. l B.2 C. 12. D.13
Đọc tiếp
Dung dịch X có chứa 0,07 mol Na+; 0,02 mol và x mol OH-. Dung dịch Y có chứa ; và y mol H+. Tổng số mol và là 0,04 mol. Trộn X với Y thu được 100ml dung dịch Z. Bỏ qua sự điện li của nước, pH của dung dịch thu được là:
A. l
B.2
C. 12.
D.13
Dung dịch X chứa 0,07 mol
Na
+
; 0,02 mol
SO
4
2
-
và x mol
OH
-
. Dung dịch Y chứa
ClO
4
-
,
NO
3
-
và y mol
H
+
, tổng số mol
ClO...
Đọc tiếp
Dung dịch X chứa 0,07 mol Na + ; 0,02 mol SO 4 2 - và x mol OH - . Dung dịch Y chứa ClO 4 - , NO 3 - và y mol H + , tổng số mol ClO 4 - và NO 3 - là 0,04. Trộn X và Y được 100 ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự diện li của H 2 O ) là
A. 12.
B. 2.
C. 1.
D. 13.
Dung dịch X có chứa 0,07 mol
Na
+
, 0,02 mol
SO
4
2
-
, và x mol
OH
-
. Dung dịch Y có chứa
ClO
4
-
,
NO
3
-
và y mol
H
+
; tổng số mol
ClO...
Đọc tiếp
Dung dịch X có chứa 0,07 mol Na + , 0,02 mol SO 4 2 - , và x mol OH - . Dung dịch Y có chứa ClO 4 - , NO 3 - và y mol H + ; tổng số mol ClO 4 - , NO 3 - là 0,04 mol. Trộn X và T được 100 ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H 2 O ) là :
A. 1.
B. 12.
C. 13.
D. 2.
Dung dịch X có chứa: 0,07 mol Na+; 0,02 mol SO42- và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4- và NO3- là 0,04. Trộn X và Y được 100ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là A. 2. B. 13. C. 1. D. 12.
Đọc tiếp
Dung dịch X có chứa: 0,07 mol Na+; 0,02 mol SO42- và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4- và NO3- là 0,04. Trộn X và Y được 100ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là
A. 2.
B. 13.
C. 1.
D. 12.
Bảo toàn điện tích đối với dung dịch X, ta có: 0,07.1 = 0,02.2 + x.1 → x = 0,03
Bảo toàn điện tích đối với dung dịch Y, ta có: y.1 = 0,04.1 → y = 0,04
Khi trộn dung dịch X và Y thì
H+ + OH- → H2O
(0,04) (0,03)
→ nH+còn dư = 0,04 – 0,03 = 0,01 mol → [H+] còn dư = 0,01/0,1 = 0,1M → pH = – lg[H+] = 1
Đáp án C
Đúng 0
Bình luận (0)
Dung dịch X có chứa: 0,07 mol Na+; 0,02 mol SO42- và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4- và NO3- là 0,04. Trộn X và Y được 100ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là A. 2. B. 13. C. 1. D. 12
Đọc tiếp
Dung dịch X có chứa: 0,07 mol Na+; 0,02 mol SO42- và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4- và NO3- là 0,04. Trộn X và Y được 100ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là
A. 2.
B. 13.
C. 1.
D. 12
Chọn C
Bảo toàn điện tích đối với dung dịch X, ta có: 0,07.1 = 0,02.2 + x.1 → x = 0,03
Bảo toàn điện tích đối với dung dịch Y, ta có: y.1 = 0,04.1 ⇒ y = 0,04
Khi trộn dung dịch X và Y thì H+ + OH- → H2O
(0,04) (0,03)
⇒ nH+còn dư = 0,04 – 0,03 = 0,01 mol ⇒ [H+] còn dư = 0,01/0,1 = 0,1M ⇒ pH = – lg[H+] = 1
Đúng 0
Bình luận (0)
Dung dịch X có chứa: 0,07 mol Na+, 0,02 mol SO42- và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4- và NO3- là 0,04. Trộn X và Y được 100ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của nước) là: A. 1. B. 12. C. 13. D. 2.
Đọc tiếp
Dung dịch X có chứa: 0,07 mol Na+, 0,02 mol SO42- và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4- và NO3- là 0,04. Trộn X và Y được 100ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của nước) là:
A. 1.
B. 12.
C. 13.
D. 2.
Đáp án A
Theo ĐL BT ĐT thì x = 0,03 mol
Theo ĐLBT ĐT thì nH+ = nClO4(-)+ nNO3(-) = 0,04 mol
H+ + OH- → H2O
0,04 0,03
nH+ dư = 0,01 mol; [H+] dư = 0,01/0,1 = 0,1 suy ra pH = 1
Đúng 0
Bình luận (0)
Trộn 400 ml dung dịch X chứa Na+, K+ và x mol OH- (tổng số mol Na+ và K+ là 0,06) với 600 ml dung dịch Y chứa 0,01 mol SO42-, 0,03 mol Cl-, y mol H+. pH của dung dịch thu được sau phản ứng là A. 1,0 B. 12,0 C. 2,0D. 13,0 D. 13,0
Đọc tiếp
Trộn 400 ml dung dịch X chứa Na+, K+ và x mol OH- (tổng số mol Na+ và K+ là 0,06) với 600 ml dung dịch Y chứa 0,01 mol SO42-, 0,03 mol Cl-, y mol H+. pH của dung dịch thu được sau phản ứng là
A. 1,0
B. 12,0
C. 2,0D. 13,0
D. 13,0
Ta có OH- 0,06 mol và H+ có 0,05 mol
=> Sau khi trộn còn dư 0,01 mol OH- và V = 1 lít
=> pH = 12
=> Đáp án B
Đúng 0
Bình luận (0)